Benefícios
A CBDL é a representante das empresas fornecedoras
do segmento de diagnóstico laboratorial.
Publicações
sobre o setor
Participação
nos Grupos
de Trabalho
Alianças
estratégicas
Acesso
ao mercado
Dados econômicos
Seja um associado e aproveite todos os benefícios que a CBDL oferece
Notícias em destaque

CBDL participa de painel sobre gestão no 15º Seminário UNIDAS
Carlos Eduardo Gouvêa, presidente executivo da Câmara Brasileira do Diagnóstico Laboratorial (CBDL), participou do "15º Seminário UNIDAS - Autogestões e suas Contribuições para a Saúde Suplementar", que ocorreu em Brasília (DF), nos dias 24 e 25 de abril. O evento,...

CBDL amplia rol de associados
Neste ano, a Câmara Brasileira de Diagnóstico Laboratorial (CBDL) conquistou mais quatro associados. Na categoria “Pleno”, que abarca a indústria,...

CBDL na Imprensa

Associados
da CBDL.

Associe-se
Notícias por categoria
CBDL participa de painel sobre gestão no 15º Seminário UNIDAS
Carlos Eduardo Gouvêa, presidente executivo da Câmara Brasileira do Diagnóstico Laboratorial (CBDL), participou do "15º Seminário UNIDAS -...
CBDL amplia rol de associados
Neste ano, a Câmara Brasileira de Diagnóstico Laboratorial (CBDL) conquistou mais quatro associados. Na categoria “Pleno”, que abarca a indústria,...
Modificação da classificação fiscal dos reagentes de diagnóstico causará grande impacto no mercado de saúde
A Câmara Brasileira de Diagnóstico Laboratorial (CBDL), entidade representativa do setor de diagnóstico in vitro (reagentes e equipamentos), acaba...
ChatGPT já supera médicos em diagnósticos e startup nacional quer tornar o processo ainda mais eficiente
Pesquisadores do Beth Israel Deaconess Medical Center, ligado à Universidade de Harvard, realizaram um estudo comparativo entre o raciocínio clínico...
Lab-to-Lab Pardini leva palestrantes para o Congiplab, o Congresso Brasileiro de Análises Clínicas
Parte do ecossistema do Grupo Fleury, o Lab-to-Lab Pardini, pioneiro e referência nacional no serviço de apoio laboratorial, acaba de declarar para...
Embragen, nova associada da CBDL, recebe diretoria da entidade para reuniões em novo espaço
Novo associada da Câmara Brasileira de Diagnóstico Laboratorial (CBDL), a Embragen, Centro Logístico Industrial Aduaneiro (CLIA), foi fundada na...
CBDL participa de Simpósio Internacional de Medicina Laboratorial promovido pela Snibe
A Câmara Brasileira de Diagnóstico Laboratorial (CBDL), em conjunto com Associação Brasileira de Medicina Diagnóstica (Abramed), a International...
Vai até 24 de abril as inscrições para propostas para Centros de Pesquisa em Inteligência Artificial Aplicada à Saúde da FAPESP
A FAPESP acaba de publicar em seu portal a Chamada de Propostas Fapesp para Centros de Pesquisa em Inteligência Artificial Aplicada à Saúde (CIAS)....
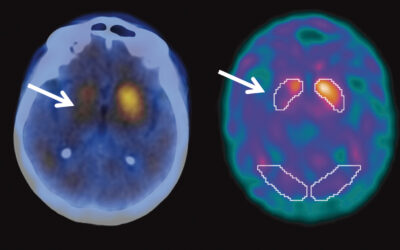
Exames de imagem são aliados na detecção de Parkinson e Alzheimer
Os quadros neurodegenerativos são condições que interferem no funcionamento do sistema nervoso de maneira crônica, afetando progressivamente a...
Testes genéticos: como eles podem contribuir no tratamento do câncer
O aumento de casos de câncer em pessoas jovens vem sendo considerado uma verdadeira epidemia global. De acordo com um estudo recente, publicado na...
Selecionadas as equipes de cientistas cuja missão é tornar ‘o mundo livre de doenças’
Acabam de ser anunciadas as 17 equipes de cientistas de 12 países que aceitaram a missão de viabilizar que no futuro próximo seja possível tornar o...
Oncoclínicas digitaliza dados de exames e prontuários em processo de transformação digital
O Grupo Oncoclínicas, uma das maiores referências no tratamento de doenças oncológicas da América Latina, está utilizando a tecnologia para coletar...
CBDL participa do Inova Day da UNICAMP
No início de abril, a Câmara Brasileira de Diagnóstico Laboratorial (CBDL), por meio de sua diretora técnica, Josely Chiarella, participou do INOVA...
CBDL planeja realização de encontros que priorizam a jornada do paciente. De como o diagnóstico foi decisivo para o acesso à terapia assertiva em uma doença rara
Carlos Eduardo Gouvêa é um dos principais líderes do segmento laboratorial no Brasil. Atualmente, ele preside a Câmara Brasileira de Diagnóstico...
O que muda com as novas regras do Conselho Federal de Medicina sobre publicidade médica?
A revisão periódica das regras de publicidade/propaganda médica é crucial devido ao aparecimento de novas tecnologias e à evolução dos meios de...
CPDI IBRACHINA/IBRAWORK E UNICAMP LANÇAM EDITAL OPEN INNOVATION DE SAÚDE. EDITAL É VOLTADO PARA PROJETOS DE INOVAÇÃO EM DIVERSAS ÁREAS DA SAÚDE HUMANA
O Centro de Pesquisa, Desenvolvimento e Inovação (CPDI) Ibrachina/Ibrawork e a Unicamp lançaram o edital Open Innovation na Saúde, voltado para...
Fórum da ABRAIDI entra oficialmente para o calendário de eventos de São Paulo
O Fórum da Associação Brasileira de Importadores e Distribuidores de Produtos para Saúde que será realizado em sua 7ª edição, em 24 de abril, na...
Mercado de produtos para a saúde abriu quase 4.500 vagas de trabalho, em 2023, apesar de ter crescido 1%
O setor de produtos médico-hospitalares andou de lado, em 2023, mas apesar disso um número expressivo de vagas no mercado de trabalho foi aberto. No...
Fulvio Facco, presidente do Conselho da CBDL, entrega prêmio Não Aceito Corrupção
O presidente do Conselho de Administração da Câmara Brasileira de Diagnóstico Laboratorial (CBDL), Fulvio Facco, representou a entidade na entrega...
Taxa de positividade em testes de influenza aumenta 200% em dois meses na maior rede de farmácias do país
As farmácias Raia e Drogasil, do grupo RD Saúde, registraram aumento na procura por testes de influenza nos primeiros meses deste ano e crescimento...
Instituto Ética Saúde elege novo Conselho de Administração
O novo Conselho de Administração do Instituto Ética Saúde foi eleito e empossado durante Assembleia Ordinária realizada no dia 15 de março, na sede...

Câmara Brasileira de Diagnóstico Laboratorial
Neste sentido, tem trabalhado em conjunto com diversas entidades atuantes no setor de diagnósticos, no Brasil e exterior, promovendo e incentivando a manutenção de elevados padrões éticos e científicos no mercado, zelando pela qualidade de seus produtos, dentro das normas exigidas internacionalmente.